EGF ( ეპიდერმისის ზრდის ფაქტორთა რეცეპტორების მოქმედების მექანიზმი და მათი როლი ონკოლოგიაში
სხვადასხვა ზრდის ფაქტორთა ErbB რეცეპტორებთან დაკავშირების შემდეგ ხდება მათი დიმერიზაცია და იწყება ტრანსფოსფორილირების პროცესი რის შემდეგაც უჯრედში ირთვება სხვადასხვა სასიგნალო გზები
ErbB რეცეპტორების ლიგანდები მრავალ უჯრედულ პროცესს არეგულირებენ მათ შორის: უჯრედული ციკლის მიმდინარეობას უჯრდის პროლიფერაციას, აპოპტოზს ცილის სინთეზს, მეტაბოლიზმსა და დიფერენცირებას ჭრილობების შეხორცებას, ახალშობილთა ზრდასა და განვითარებას აგრეთვე ქსოვილთა წარმოქმნას.
ErbB რეცეპტორების სიგნალიზაციის ცვლილება ონკოგენეზის მიზეზი ხდება იწვევს რა ინტენსიურ პროლიფერაციასა და ზრდას, აპოპტოზის პროცესების დათრგუნვის პარალელურად რის წყალობითაც აქტიურდება მეტასტაზირებისათვის აუცილებელი პროცესები როგორიცაა ინვაზია მიგრაცია და ნეო-ანგიოგენეზი.
1.1 ErbB რეცეპტორები და მათი სტრუქტურა
ეპიდერმული ზრდის ფაქტორის რეცეპტორი (EGFR/HER1) და ამავე ოჯახის სხვა წევრები (c-ErbB2/HER2/neu, ErbB3/HER3 და ErbB4/HER4) წ 160–190 კდას ზომის ტრანსმემბრანულ (I ტიპის) თიროზინ-კინაზური რეცეპტორებია თითოეული მათგანი შედგება: ექსტრაცელულარული ლიგანდშემაკავშირებელი ცისტეინით მდიდარი დომენებისგან, ტრანსმემბრანული რეგიონისაგან და უჯრედშიდა კინაზური დომენისგან C ტერმინალური ბოლოთი რომელიც აუცილებელია რეცეპტორის აქტივობის რეგულირებისთვის. EGFR იყო ამ ოჯახის პირველი იდენტიფიცირებული წევრი; ეს არის 170 კდა ზომის გლიკოპროტეინი. რეცეპტორის ზრდის ფაქტორის ლიგანდთან (ეპიდერმული ზრდის ფაქტორი, EGF) გამოყოფა პირველად 1979 წელს შეძლეს. (McKanna და სხვ.).ERbB2 ErbB3 ჰეტეროდიმერიზაციის შემდეგ რეცეპტორთა ERbB2 ბოლო ააქტივებს MAP კასკადს ხოლო ErbB3 კი PI3K/AKT კასკადს
რაც განპირობებულია თიროზინკინაზურ რეცეპტორთა კატალიზურ დომენში არსებულ ამინომჟავათა განსხვავებებით. ErbB3 ლიგანდით აქტივაციის შემდეგ როგორც უკვე აღვნიშნეთ აქტივდება PI3K/AKT სასიგნალო გზა.
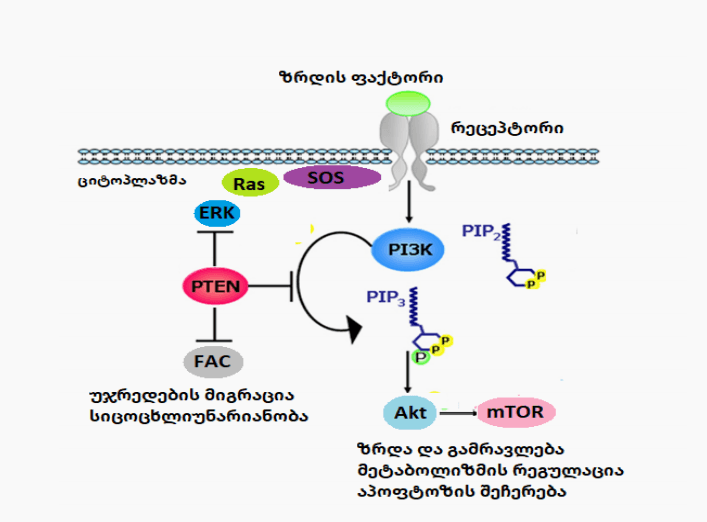
ამ დროს PI3K გარდაქმნის PIP2-ს PIP3-ად. ამ პროცესის შედეგად პროტეინკინაზა B (AKT) გადაადგილდება უჯრედის მემბრანისაკენ იცვლის კონფორმაციას და ფოსფატიდილინოზიტოლდამოკიდებული პროტეინკინაზა 1 (PDK1) საშუალებით აქტივდება. მისი აქტივაცია იწვევს ისეთი ცილების ფოსფორილირებას როგორიცაა FOXO და mTORC1 ამ პროცესების ინჰიბიტორს წარმოადგენს ფოსფატაზა ცილა PTEN რომელიც PIP3 ისევ PIP2-ად გარდაქმნის და ამით აინჰიბირებს პროტეინკინაზა AKT-ს. PTEN ცილის ფუნქცია მხოლოდ პროტეინკინაზა B ინჰიბირება არ არის არამედ MAPK/ERK სასიგნალო გზასაც რითაც ის აჩერებს უჯრედის პროლიფერაციის პროცესს და ასევე FAK ცილას რომელიც Src ცილების ოჯახს მიეკუთვნება და უჯრედების მიგრაციას უწყობს ხელს ის დიდ როლს თამაშობს სხვადასხვა ტიპის სიმსივნეების მეტასტაზირების პროცესში. ამრიგად PTEN ფიზიოლოგიურ პირობებში მნიშვნელოვანი რეგულატორის როლს ასრულებს. PI3K/AKT პარალელურად თიროზინკინაზური რეცეპტორის კატალიზურ დომენთან სხვადასხვა შუალედური ცილები Grb2/SOS წარმოქმნიან კომპლექსებს რის საშუალებითაც ინფორმაცია Ras ცილას გადაეცემა რომელიც GTP მიერთების შემდეგ აქტივდება ჩამოსცილდება აღნიშნულ კომპლექსს და ააქტივებს Raf ცილას რომელიც თავის მხრივ კიდევ ერთ კინაზას ააქტივებს ეს კი MAP კინაზას შედეგად კიდევ ერთი სასიგნალო გზა MAP კასკადი ირთვება ის სხვადასხვა ტრანსკრიპციის ფაქტორების აქტივაციასა და რიბოსომული ცილების სინთეზს აჩქარებს და უჯრედი ინტერფაზიდან მიტოზის ფაზაში გადაჰყავს.ირთვება JAK/STAT სასიგნალო გზაც რომელიც ასევე უჯრედის პროლიფერაციას უწყობს ხელს.
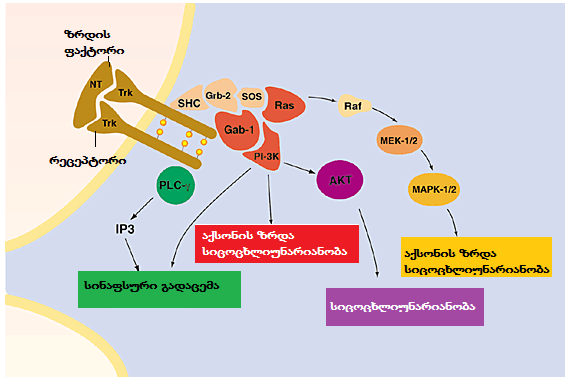
ErbB რეცეპტორთა ექსპრესიისა და ფუნქციის დისრეგულაცია სიმსივნის მრავალი ტიპისთვისაა დამახასიათებელი მათ შორის მკერდის საკვერცხის ტვინის კუჭ-ნაწლავის ტრაქტისა და პროსტატის სიმსივნეების დროს.დისფუნქციის გამომწვევი რამოდენიმე მექანიზმი არსებობს ესენია:მუტაციები,რეცეპტორთა ადაპტორულ ცილათა და ლიგანდთა გაძლიერებული ექსპრესია ისევე როგორც სასიგნალო გზებში მონაწილე სხვადასხვა კომპონენტების ლოკალიზაციის ცვლილება.მკერდის სიმსივნის ერთ-ერთი ფორმის მაღალი გრადაციის დუქტალური კარცინომის დროს აღინიშნება ErbB2,რეცეპტორთა ჰიპერექსპრესია.მაშინ როდესაც მკერდის კეთილთვისებიანი სიმსივნეების არსებობის დროს ამ რეცეპტორთა რაოდენობა მკვეთრად მცირდება.საერთო ჯამში ErbB2 რეცეპტორთა ჰიპერექსპრესია მკერდის სიმსივნეების შემხვევათა დაახლოებით 25-30% აღინიშნება.ასევე აუცილებელია აღვნიშნოთ,რომ კვლევების შედეგები აჩვენებს,რომ მისი ჰიპერექსპრესია ვითარდება უშუალოდ პათოლოგიური პროცესების მიმდინარეობის პარალელურად.გარკვეული მტკიცებულებები არსებობს იმის შესახებაც,რომ HER2 ჰიპერექსპრესია სიმსივნური უჯრედების მეტასტაზირებას უწყობს ხელს. ნეოპლასტიური ტრანსფორმაციისათვის მხოლოდ HER2/ErbB2 ჰიპერექსპრესია და დიმერიზაცია საკმარისი არ არის საჭიროა მათი ErbB3 კოექსპრესია თუმცა ნაწილობრივ ტრანსფორმირებულ უჯრედებში HER2 ჰომოდიმერების ჰიპერექსპრესია უჯრედის პროლიფერაციას უწყობს ხელს.აღსანიშნავია ისიც,რომ HER2 HER2 ჰომოდიმერები წარმოიქმნება ლიგანდის არსებობის გარეშეც.გარდა ამისა ამ რეცეპტორს სხვა ჰომოლოგიურ ცილებთან მაგალითად ErbB2 თან მაღალი აფინობით წარმოქმნის დიმერებს რაც თავისთავად ნიშნავს იმას,რომ HER2 ჰიპერექსპრესია ზრდის ნეოპლასტიკური ტრანსფორმაციისა და სიმსივნური უჯრედების მეტასტაზირების რისკს.EGFR გენის ამპლიფიკაცია და რეცეპტორის პათოლოგიური ჰიპერექსპრესია საკვერცხისა და ეპითელურ სიმსივნეთა 70%-შია ჰიპერექსპრესირებული.თუმცა ამ ოჯახის ყველა რეცეპტორის ჰიპერექსპრესია სიმსივნის წარმოქმნასთან დაკავშირებული არ არის.ErbB4 ზოგიერთი სიმსივნის დროს ანტიონკოგენის როლს ასრულებს თუმცა აღნიშნულ საკითხთან დაკავშირებით კვლევის გაგრძელებაა აუცილებელი.კვლევის შედეგების მიხედვით,რომელიც ჩატარდა ალესია მორატოს მიერ 2023 წელს ნათელი ხდება,რომ ERBB რეცეპტორებს შეუძლიათ STAT ცილების აქტივაციაც როგორც პირდაპირი მოქმედების შედეგად ისე JAK კინაზას დახმარებით.ფოსფორილირების შემდეგ ისინი უჯრედის ბირთვში ტრანსლოცირდებიან.სხვადასხვა STAT ცილებს ექსპრესიის განსხვავებული პატერნები და უჯრედული პროცესების რეგულაციის სხვადასხვა უნარი აქვს.STAT/EerbB ინტერაქცია ფიზიოლოგიურ პირობებში მნიშვნელოვანია ლობულოალვეოლარული განვითარებისათვის ასევე პროლაქტინის გენთა ექსპრესიისათვის რაც შემდგომში ლაქტაციის პროცესისათვის არის გადამწყვეტი.Erbb3 და Erbb4 რეცეპტორების არმქონე თაგვებმა გამოავლინეს STAT5 დისფუნქცია რამაც გამოიწვია ლობულოალვეოლარული განვითარების დეფექტები და პროლაქტინის მაკოდირებელი გენების ექსპრესიის დაქვეითება. ErbB4 აღნიშნული პროცესების ძლიერ აქტივატორს წარმოადგენს რაც შეეხება ErbB3 მისი ფიზიოლოგიური როლი ბოლომდე გარკვეული არ არის თუმცა სავარაუდოა რომ ის ლობულოალვეოლარული განვითარების გარკვეული ეტაპების დასრულების შემდეგ აპოპტოზის პროცესში მონაწილეობს და მისი მუტაცია მკერდის მრავალი ტიპის სიმსივნის დროს გვხვდება.
გამოყენებული ლიტერატურა
Alessia Morato, Paolo Accornero Russell C. Hovey Journal of Mammary Gland Biology and Neoplasia (2023) 28:10 ERBB Receptors and Their Ligands in the Developing Mammary Glands
of Different Species: Fifteen Characters in Search of an Author
Cancer Cell Signalling Edited by
Amanda Harvey
Biosciences, Brunel University, London, UK
"უჯრედული პროცესების რეგულაციის პრინციპები" დ.მიქელაძე ნ.ნაცვლიშვილი