BDNF მოქმედების მოლეკულური მექანიზმი
თავის ტვინის ნეიროტროპული ფაქტორი სხვებთან შედარებით ყველაზე დიდი რაოდენობით გვხვდება ზრდასრული ადამიანის თავია ტვინში და ასრულებს როგორც ზრდის ფაქტორის ისე ნეირომოდულატორის როლს. ამით მას ნეირონთა განვითარებაში, სინაპსურ პლასტიურობასა და კოგნიტური ფუნქციის ჩამოყალიბებაში მთავარი ფუნქცია აკისრია.კვლევები აჩვენებს,რომ თავის ტვინის ნეიროტროპულიფაქტორის სინთეზი რომელ სტადიური პროცესია თავდაპირველად ენდოპლაზმურრეტიკულუმზე სინთეზდება პრეპრო BDNF რის შემდეგაც ხდება პრო BDNF Სინთეზი აღნიშნული ცილა შედგება 118 C ტერმინალური და 129 N ტერმინალური დომეინისაგან.სინთეზის მომდევნო სტადიაზე ეს უკანასკნელი ისევ იყოფა და წარმოიქმნება თავის ტვინისნეიროტროპული ფაქტორი BDNF და ProBDNF ფარმაკოლოგიური ეფექტი გააჩნიათმხოლოდ მას შემდეგ რაც ისინი გამოვლენ უჯრედგარეთ. აღსანიშნავია ის ფაქტიც რომ ამორი ნივთიერების დონე სხვადასხვა ასაკში ადამიანის თავის ტვინის სხვადასხვა უბანშიგანსხვავებულია ბავშვობის პერიოდში ბევრად მეტია პრო-BDNF ზრდასრულობაში BDNF გარდა ამისა გადამწყვეტი მნიშვნელობა ენიჭება გენეტიკურ პოლიმორფიზმს კერძოდ Metჩანაცვლებას Val ით 66 დომეინზე.პრო-BDNF ურთიერთქმედებს P-75NRT რეცეპტორთან რომელიც მიეკუთვნება TNF სიმსივნის ნეკროზული ფაქტორის ჯგუფს.ასევე ის ურთიერთქმედებს ცილა სორტილინთან და ცილა VSP 10-თან.Რაც შეეხება თავის ტვინის ნეიროტროპულ ფაქტორს ის ურთიერთქმედებს თიროზინკინაზა B-სთან რომელიც მიეკუთვნება თიროზინკინაზების ჯგუფს.მოსვენებულ მდგომარეობაში ორივე ტიპის რეცეპტორი უჯრედშიდა ვეზიკულებშია განთავსებული cAMP, Ca2+ ან ელექტრული იმპულსითსტიმულაციის შემდეგ ეს ცილები გამოთავისუფლდება უჯრედშიდა ვეზიკულებიდან დაერწყმის უჯრედის მემბრანას.პრო-BDNF/P75NRT/sortilin კომპლექსი იწვევს სამ სხვადასხვა ეფექტს:პირველ შემთხვევაში აღნიშნული კომპლექსი ურთიეთქმედებს C--Jun კინაზასთან რისშედეგადაც ხდება ნერვული უჯრედების აპოპტოზი მაგრამ ამასთანავე ის -Jun კინაზასთან რისშედეგადაც ხდება ნერვული უჯრედების აპოპტოზი მაგრამ ამასთანავე ისურთიერთქმედებს RhoA-სთნ და NF-KB -სთან ისინი პასუხისმგებელნი არიან ნერვული უჯრედების დიფერენციაციაზე და ნეიროპლასტიურობაზე. (Przemysław Kowianski1,2 •Grazyna Lietzau 2018)
2022 წელს აჰმად ბაძარის ხელმძღვანელობით ჩატარებული კვლევების მიხედვით დგინდება,რომ თავის ტვინის ნეიროტროპული სამიზნე თიროზინკინაზური რეცეპტორების სამი სხვადასხვა იზოფორმა არსებობს რომელიც ერთი და იმავე გენის სამი სხვადასხვა სპლაისური ვარიანტით კოდირდება ესენია სრული სიგრძის იზოფორმა (TrkB-FL) და მოკლე იზოფორმები რომელთაც უჯრედშიდა კატალიზური დომენი არ გააჩნიათ (TrkB-T1) და (TrkB-T2 ) TrkB-T1 იზოფორმას ძირითადად ინჰიბიტორის ფუნქცია აქვს ასევე მასზეა დამოკიდებული ციტოჩონჩხის სწორი ორგანიზაცია. სპლაისური ვარიანტების ექსპრესია მკვეთრად განსხვავდება უჯრედების ტიპის მიხედვით TrkB-T1 ექსპრესია გლიურ უჯრედებში დაახლოებით 100-ჯერ მეტია ვიდრე ნეირონებში. ასტროციტებში TrkB-T1 კავშირს გლიურ უჯრედებსა და ასტროციტებს შორის კავშირს ინოზიტოლტეიფოსფატის საშუალებით ამყარებს რომელიც თავის მხრივ გლიურ უჯრედებში კალციუმის კონცენტრაციის გაზრდის ხარჯზე წარმართავს სხვადასხვა პროცესებს.ამის საშუალებით ის ასტროციტების მორფოგენეზსაც განსაზღვრავს პასუხისმგებელია ჰომეოსტაზისა და გლუტამატის უკუმიტაცების პროცესებზეც.გლიოგენეზის დროს ის ააქტივებს G ცილებს და ამასთანავე პროტეინკინაზა C-საც. რის ხარჯზეც ხდება გლიური უჯრედების ჩამოყალიბება.TrkB-T1 ასევე აფერხებს ასტროციტების მიერ გლიცინის შეთვისებას მისი ტრანსპორტერების ენდოციტოზის ხარჯზე. ნეირონებში TrkB-T1 ფუნქცია ბოლომდე შესწავლილი არ არის თუმცა კვლევის შედეგები აჩვენებს,რომ ამ რეცეპტორთა დეფიციტი გრძელვადიანი პოტენციაციის დარღვევას იწვევს ამ შემთხვვაში ნეირიტების ზრდა ფერხდება და ცხოველებში შეინიშნება შფოთი და დეპრესიის მსგავსი ქცევა. რაც შეეხება TrkB-T2- რეცეპტორს მის შესახებ ძალიან ცოტა რამ არის ცნობილი თუმცა ის აფერხებს TrkB-FL. სრული სიგრძის რეცეპტორების ეფექტებს. დასკვნის სახით შეიძლება ვთქვათ,რომ TrkB-T1,და TrkB-T2 ცვლიან TrkB-FL ეფექტებს და მრავალი ფსიქიკური დაავადების დროს მათი თანაფარდობა ირღვევა.
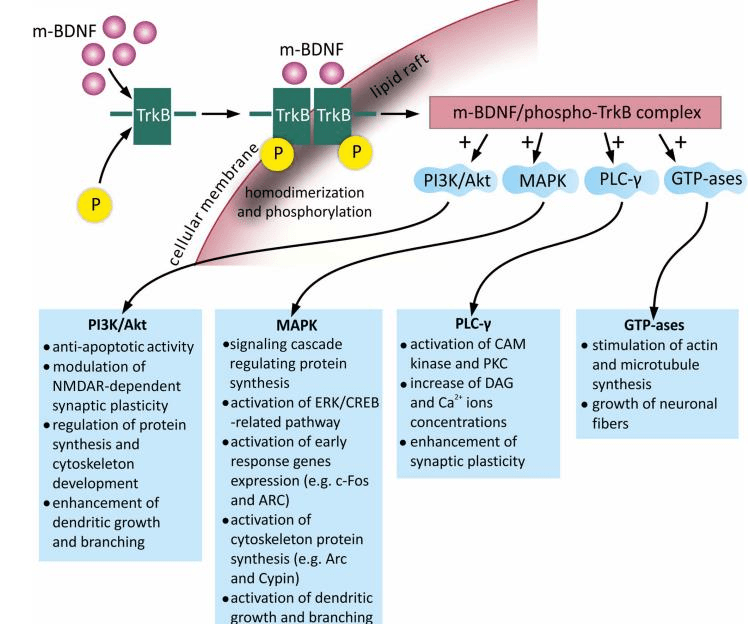
თავის ტვინის ნეიროტროპული ფაქტორი ააქტივებს PI3K/Akt- mTOR სასიგნალო გზასაც
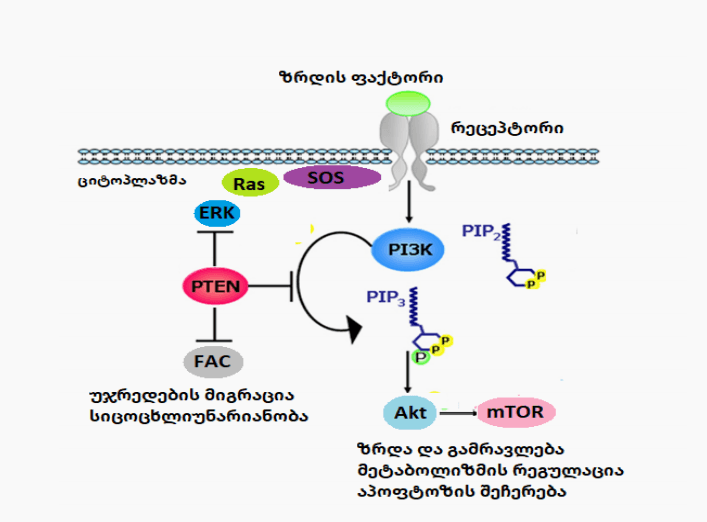
რაც აძლიერებს ცილების სინთეზს და ხელს უწყობს ნეირიტების ზრდას ეს სასიგნალო გზა წამყვან როლს ასრულებს სხვადასხვა ნაერთებისა და ფერმენტების მეშვეობით გამოწვეული ნეიროპროტექტორული ეფექტის განვითარებაში.როგორიცაა ქვერცეტინი კურკუმინი და ჰემოქსიგენაზა, სწორედ ამ სასიგნალო გზის აქტივაცია იწვევს სწორედ ამიტომაა რომ თავის ტვინის ტრამვის შემდეგ გლუტამატის უკუმიტაცება იზრდება და ამ ნივთიერების ციტოტოქსიური ეფექტები ასე თუ ისე მცირდება. გარდა ამისა PI3K/Akt სასიგნალო კასკადის აქტივაციის წყალობით (PSD-95) ტრანსლოკაცია ძლიერდება რაც პოსტსინაპსური სიმკვრივის სწორ ორგანიზაციას უწყობს ხელს. ამ პროცესს ჰიპერგლიკემია აფერხებს. აღსანიშნავია ისიც,რომ ნსულინრეზისტენტული მეორე ტიპის დიაბეტის დროსაც შეფერხებულია Akt ფოსფორილირება რაც ნეიროგენეზის შეფერხებას უწყობს ხელს. ამ პროცესის აქტივაცია ნეირონთა სწორი მორფოგენეზისათვის უმნიშვნელოვანესია თუმცა მისი სწორი წარმართვისათვის MAP- კასკადის აქტივაციაა აუცილებელი. თიროზინკინაზური რეცეპტორების აქტივაციის შედეგად PI3K/Akt- სასოგნალო გზის პარალელურად აქტივდება MAP-კასკადი აღსანიშნავია,რომ MAP კინაზას განსხვავებული იზოფორმები უჯრედში განსხვავებულ ფუნქციებს ასრულებს ამ კასკადის აქტივაციით კონტროლდება უჯრედული ციკლის ნორმალური მიმდინარეობა, ფერხდება აპოპტოზის პროცესი, ამ პროცესის აქტივაცია განაპირობებს ანტეროგრადული სიგნალების წარმოშობას დენდრიტებიდან სომასკენ გარდა ამისა MAP-კასკადის აქტივაცია ხელს უწყობს ამპა რეცეპტორების გაძლიერებულ გადმოტანას უჯრედის მემბრანისაკენ ამით რათქმაუნდა ძლიერდება რიგი სინაპსებისა და იცვლება სინაპსური პლასტიურობა საინტერესოა ის ფაქტი რომ სხვადასხვა კვლევების შედეგები აჩვენებს,რომ Nucleus accumbens-ში თავის ტვინის ნეიროტროპული ფაქტორის მოქმედება ორგვარია ერთის მხრივ შესაძლებელია პროტეინკინაზა Erk ინტენსიური ფოსფორილირების ხარჯზე მოიმატოს ამპა რეცეპტორების რაოდენობამ მემბრანაზე რაც ხელს შეუწყობს გრძელვადიანი პოტენციაციის განვითარებას ხოლო მეორეს მხრივ შესაძლებელია მოხდეს ამ რეცეპტორთა მკვეთრი დაუნრეგულაცია. აუცილებელია ითქვას რომ BDNF ერთ-ერთი ეფექტი ცილა CREB-ის აქტივაციაა რომელიც დნმ-ის გარკვეულ თანმიმდევრობას უკავშირდება და ნეირონთა აქსონების ზრდას უწყობს ხელს. მესამე სისტემა რომელიც აქტიურდება თავის ტვინის ნეიროტროპული ფაქტორის წყალობით არის ფოსფოლიპაზა C რომლის აქტივაციას PIP2-ის IP3-ად და DAG-ად გარდაქმნა მოჰყვება IP3 უკავშირდება ენდოპლაზმურ ბადეზე მდებარე სპეციალურ რეცეპტორებს და იწვევს კალციუმის კონცენტრაციის მომატებას ციტოპლაზმაში. ხოლო დიაცილგლიცეროლი იწვევს პროტეინკინაზა C აქტივაციას რაც ხურავს კალიუმის არხებს და მათი მოდულაციის ხარჯზე იწვევს მოქმედების პოტენციალის ცვლილებას. რაც შეეხება კალციუმს ის პირველ რიგში ააქტივებს CAM კინაზა II და ამით ხელს უწყობს სინაპსური პლასტიურობისა და კოგნიტური ფუნქციების გაუმჯობესებას რაც შეეხება პროტეინკინაზა C აქტივაციას ეს ხელს უწყობს არამარტო მოქმედების პოტენციალის ცვლილებას არამედ ნეირონების ზრდასა და დიფერენცირებას ნმდა და ა,[ა რეცეპტორების ფოსფოეილიეებას და გაემ A რეცეპტორების სინთეზს და მეხსიერების კონსოლიდაციას.(Amjad H. Bazzari 2022) 2018 წელს ამერიკაში ნორთვესტერნის უნივერსიტეტის ნეიროფიზიოლოგიის
დეპარტამენტში პატრიკ ლიუსა და რობინ ნუსლოკის ხელმძღვანელობით ჩატარდა კვლევა სადაც შეისწავლეს ვარჯიშის შედეგად განპირობებული ნეიროგენეზის პროცესის დროს მიმდინარე ფიზიოლოგიური პროცესები. კვლევის შედეგად დადგინდა,რომ ვარჯიშის
დადებითი ნეიროპროტექტორული ეფექტები დაკავშირებულია ჰიპოკამპის მიდამოში გაძლიერებულ ნეიროგენეზთან, რასაც განაპირობებს სისტემატური ვარჯიშის დროს თავის ტვინის ნეიროტროპული ფაქტორის ინტენსიური გამოყოფა. აღსანიშნავია,რომ მღრღნელების შემთხვევაში ექსპერიმენტის ჩატარების შემდეგ მკვეთრად გაუმობესდა
მათი მოძრაობის უნარი რაც მიუთითებს BDNF წამყვან როლზე ნეიროგენეზის პროცესში. ხაზი უნდა გავუსვათ იმ ფაქტს რომ თავის ტვინის ნეიროტროპული ფაქტორი დადებითად
მოქმედებს პაციენტების კოგნიტიურ ფუნქციაზეც. თუმცა ადამიანის თავის ტვინის და ექსპერიმენტული კვლევების სირთულიდან გამომდინარე აუცილებელია კვლევების გაგრძელება ჯანმრთელ მოხალისეებზე რადგან ბევრი რამ ჯერ კიდევ არ არის ბოლომდე
შესწავლილი. აღსანიშნავია რომ გადამწყვეტ როლს ჯანმრთელი მოხალისეებისა თუ
პაციენტების შემთხვევაში გენეტიკური პოლიმორფიზმი ასრულებს რაც კიდევ უფრო ართულებს ექსპერიმენტულ კვლევებს. (Patrick Z. Liu* and Robin Nusslock 2018) აღსანიშნავია რომ არსებობს მთელი რიგი ნაერთი ლიდერებისა რომლებიც ენდოგენურად ვარჯიშის დროს ან მის შემდეგ გამოიყოფა და აძლიერებს თავის ტვინის ნეიროტროპული ფაქტორის ექსპრესიას.2019 წელს ლაურეტ ელ ჰაიეკის ხელმძღვანელობით ჩატარდა კვლევა სადაც დადგინდა,რომ ლაქტატი აძლიერებს სირტუინ-1 დეაცეტილაზას იგივე SIRT-1 ექსპრესიას და BDNF
ტრანსკრიფციის კოფაქტორის FDC5 გამოყოფას რაც იწვევს BDNF ექსპრესიის გაძლიერებას ეს შედეგი საშუალებას გვაძლევს განვიხილოთ ლაქტატი როგორც ლიდერი ნაერთი სხვადასხვა ნევროლოგიური და ფსიქიკური დაავადებების დროს.(Lauretta El Hayek,1 Mohamad Khalifeh,1) სამწუხაროდ დღესდღეისობით ფარმაცევტულ ბაზარზე არ არსებობს მედიკამენტი რომელიც ხელს შეუწყობს ნეიროგენეზის სრულყოფას სამწუხაროა ის ფაქტი რომ მთელი რიგი ნევროლოგიური დაავადებების განკურნება შესაძლებელია მხოლოდ და მხოლოდ ნეიროგენეზის სრულყოფის ხარჯზე რისთვისაც სასურველია ახალი მედიკამენტების შექმნა ისეთი ნაერთების ლიდერებად განხილვა როგორიცაა ლაქტატი კეტამინი ან თვითონ BDNF საშუალებას გვაძლევს შევიმუშავოთ განსხვავებული ქიმიური სტრუქტურის უსაბრთხო ეფექტური მედიკამენტები და სრულვყოთ ნეიროგენეზის პროცესი.
გამოყენებული ლიტერატურა
1.Amjad H. Bazzari 2022 Firas H. Bazzari 2 Int. J. Mol. Sci. 2022, 23, 8417. BDNF Therapeutic Mechanisms in Neuropsychiatric Disorders
2.Lauretta El Hayek,1 Mohamad Khalifeh,1 Victor Zibara,1 XRawad Abi Assaad,1 XNancy Emmanuel,1 Nabil Karnib,1
3.Patrick Z. Liu* and Robin Nusslock Frontiers in Neuroscience February 2018 | Volume 12
Exercise-Mediated Neurogenesis in the Hippocampus via BDNF
4.Przemysław Kowian ́ski1,2 • Grazyna Lietzau _ 1 • Ewelina Czuba1 • Monika Was ́kow2 •
5.Aleksandra Steliga2 • Janusz Morys ́ Cell Mol Neurobiol (2018) 38:579–593 / Published online: 16
6.June 2017 BDNF: A Key Factor with Multipotent Impact on Brain Signalingand Synaptic Plasticity
7.ნ.ნაცვლიშვილი დ.მიქელაძე "უჯრედული პროცესების რეგულაციის ძირითადი პრინციპები"